
巨大色素性母斑
巨大色素性母斑とは
色素性母斑(しきそせいぼはん)は、小さいものは「ほくろ」と呼ばれる茶色〜黒色のあざ(できもの)です皮膚の中に母斑細胞といわれる細胞が存在し、母斑細胞がメラニン色素を産生するために生じます。先天性巨大色素性母斑は産まれた時から存在する大きな色素性母斑で、大人になったときに直径20cm以上(1歳時点での目安は体幹で6cm、頭部・顔面では9cm以上)になる場合に巨大と定義されています。巨大色素性母斑を小さい色素性母斑と区別する理由は、巨大色素性母斑では、悪性黒色腫(ひふの癌)が数%程度で発生することがあるからです。また、中枢神経(脳や脊髄)にも母斑細胞が存在することがあります。先天性巨大色素性母斑の患者さんの数について正確な統計はありませんが、出生2万人に1人程度とされており、日本での出生数が年間約100万人とすると毎年50人程度の患者さんが産まれていることになります。
巨大色素性母斑の治療
巨大色素性母斑の治療は、手術で母斑を完全に切除することが原則です。母斑を完全に切除できれば悪性黒色腫の発生もなくなります。手術は、数回に分けて切除する分割切除術や組織拡張器(シリコンバック)を皮下に埋入し、数ヶ月かけて皮膚を拡張させた皮膚を用いて再建を行う方法、患者さんの皮膚を採取し移植する植皮手術がよく行われます。また、人工皮膚(二層性人工真皮)を皮膚移植に併用することもあります。これら従来の方法では、手術の身体的負担、母斑切除部の長いきずあと、皮膚を採取した部分にきずあとがのこる、などの問題があります。また、体表の数10%以上といった特に大きな母斑ではそもそも完全に切除してしまうことは困難です。切除手術以外の治療法としてキュレッテージという手術方法があります。皮膚は表皮(表層にある0.1mmから0.2mm程度の部分、外界から体内を保護する役割)と真皮(表皮の下層にある1mm程度の強い支持組織)から成り立っています。母斑はもともと表皮部分で発生し、成長と共に徐々に深い層まで移動する性質があります。従って、生後できるだけ早い時期がよいのですが、1歳頃までであれば、器械をもちいて母斑の表面を削り取る(キュレッテージ)と母斑細胞を高率に除去することができます。ただし、キュレッテージは症例毎に削り取れる層が異なるので、効果がある場合と効果があまりない症例があります。また母斑に生えている毛を取り除くことはできません。また、キュレッテージを行うとその部分は皮膚が部分的になくなった状態、つまりやけどをしたのと同じ状態になりますので、あまり大きい範囲は体への負担が大きく一度には実施できません。手術以外の治療にはレーザー治療がありますが、レーザーは色素を破壊する方法で直接母斑細胞を破壊するわけではありません。また、レーザーは皮膚の深部までは届きませんので、母斑細胞を完全に取り除くことは困難です。特に獣毛性母斑という毛の多い母斑では母斑に存在する毛包(毛の根元)から再発することが多いです。 以上のように、残念ながら巨大色素性母斑の治療方法は現状で確立されていません。ただし、キュレッテージやレーザー治療などの母斑細胞が残ってしまう治療を行っても、悪性黒色腫の発生頻度が上昇した、という報告はありません。つまり、母斑細胞をゼロにすることはできなくても、母斑細胞の数を減らすことで悪性黒色腫の発生を抑制していると考えられます。以上が現在の巨大色素性母斑治療の状況ですので、母斑の存在する部位や大きさ、年齢によって治療法を選択し、治療法を組み合わせて行われています。最近は、冷凍処理も注目されており、冷凍処理機器を用いた悪性腫瘍の治療も保険収載されています。色素性母斑治療にも以前からドライアイスを用いた冷凍治療が行われており、この治療も併用療法の一つとして行っています。
自家培養表皮を用いた皮膚再生治療
最近、細胞や人工材料をもちいて組織を作り出す再生医療が注目を浴びています。皮膚再生は最も古くから再生医療が行われている分野です。切手大の患者さん自身の皮膚から、1ヶ月弱で体全体を覆うことができるくらい大きな表皮を作る技術が1970年代に確立され、1980年代には患者さんへの治療が行われています。この治療は世界各国で用いられており、日本でも2009年よりこの培養技術を用いて作製される自家培養表皮(ジェイスⓇ、(株)ジャパン・ティッシュ・エンジニアリング)が重症熱傷治療に保険適用され、重症熱傷患者さんの救命に役立っています。そして、この自家培養表皮が、2016年12月から巨大色素性母斑の患者さんにも保険治療として使えるようになりました。公的保険が適用され、巨大色素性母斑治療に自家培養表皮が使用できるのは世界で日本だけです。現在までに自家培養表皮ジェイスⓇは、重症熱傷治療で約1000例以上、巨大色素性母斑治療で200例以上の患者さんに使用されています(症例数は当院推計:正確な症例数は未公表)。 自家培養表皮については以下のサイトをご覧ください。
株式会社ジャパン・ティッシュ・エンジニアリング(J-TEC)
・患者さま向け情報 「自家培養表皮によるあざ(母斑)の治療」
http://www.jpte.co.jp/Patients/giant_nevi.html
・自家培養表皮とは
http://www.jpte.co.jp/business/regenerative/cultured_epidermis.html
自家培養表皮だけで皮膚の再生が行えれば理想的なのですが、母斑を全部切除して皮膚が全くなくなってしまった場合、自家培養表皮だけで傷を治すのは困難です。皮膚は表皮と真皮からでいていますが、表皮は真皮のない場所には生着しにくいからです。ここで、上述のキュレッテージと自家培養表皮を併用すればそれぞれの問題点を補うよい治療法になるのではないかと考えられています。また、各種レーザー治療、ドライアイス治療も行っています。
現在の巨大色素性母斑の治療方針
上に述べたように巨大色素性母斑の治療は確立していません。また、母斑を全層で切除した場合、自家培養表皮だけで傷を治すことはできません。従って、現在の治療方針として以下の方針で行っています。1歳以下の方で、何回か切除しても切除できない大きさの母斑、あるいは切除しにくい場所(顔面など)にある母斑のある方は、できるだけ早期(生後3ヶ月程度から)にキュレッテージを行います。母斑が小さい時は自家培養表皮を使う必要はありませんが、大きい場合や顔面など早くきれいに直す必要がある部位では自家培養表皮を使用します。てのひらの大きさがその患者さんの体全体の面積の約1%になりますが、自家培養表皮を用いる場合は体表面積の5-10%程度まで一度の手術でキュレッテージを行うことが可能です。全身麻酔下での手術がある程度安定してできるようになるのは生後3ヶ月程度からになりますので、3ヶ月で手術を行う場合は生後1-2ヶ月で皮膚を採取しています(局所麻酔で15分程度)。できるだけ早くキュレッテージを行う理由は、早く行う方が母斑が取れやすいことと、大きな面積の母斑の方の場合、1歳までに数回以上手術を行えますので、体表面積の数10%以上のかなり大きな母斑でもキュレッテージ可能となるからです。キュレッテージの際に、脱毛レーザーを用いた脱毛処置も行います。キュレッテージを行ったあとは3ヶ月から半年程度は傷の遮光、圧迫、保湿などを行います。色調は薄くなることが多いですが、キュレッテージした部分が盛り上がって目立つ、皮膚の性質が周囲と異なる、母斑が再発する、剛毛が残り目立つ、こともあります。必要な時は、レーザー治療を追加することもあります。このような部位には、ドライアイス治療やレーザー照射を優先することもあります。切除手術などを行う場合は1歳以降に行います。 1回で切除できる場合や数回に分けて切除する場合、1歳以降に切除手術を開始します。
1回で切除できる場合や数回に分けて切除する場合、1歳以降に切除手術を開始します。1歳以降になるとキュレッテージを行うことは困難になりますが、母斑を生検(数ミリ切除して検査する)し、母斑の深さがさほど深くない場合は、母斑を器械で薄く削り、自家培養表皮を用いた治療を行うこともあります。ただし、基本的にはキュレッテージはできませんので、切除手術、エキスパンダー(皮膚を進展させるシリコンバック)を用いた再建手術などを行います。体幹部や上下肢では1歳半くらいから、顔面、頭部へのエキスパンダーの使用は骨が癒合するのを待って2歳前くらいから行います。キュレッテージを行っておくと、エキスパンダーを用いた再建を行う場合でも、切除しないといけない母斑の範囲が小さくなりますので、手術が行いやすくなります。
小学校入学以降の方、成人の方の場合は、以降切除、エキスパンダーを用いた治療、皮膚移植など患者さんご本人の予定あるいは希望に合せて治療を行います。皮膚移植を行う際に自家培養表皮を併用し、採取したご自分の皮膚の数倍以上の範囲の皮膚を再生させることも可能です。
これまで自家培養表皮を用いた母斑治療は、キュレッテージとの併用、自家皮膚移植との併用、また以下に示す臨床研究などもふくめると私が執刀した症例で100例以上の方に実施しています。
頭部巨大色素性母斑をキュレッテージと自家培養表皮で治療した症例
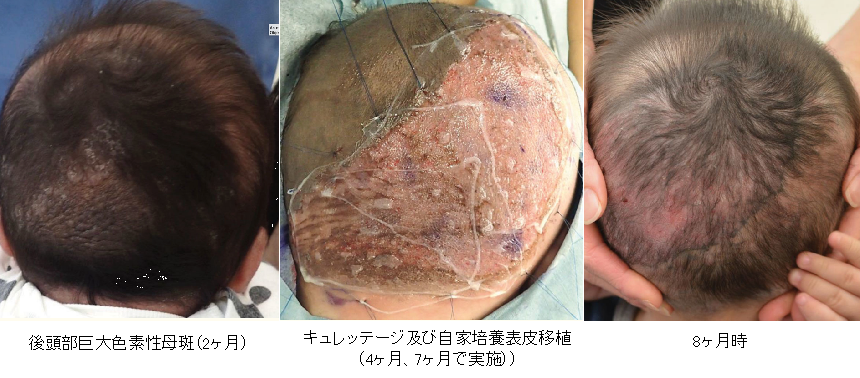
Maeda T, Morimoto N, Kakudo N, Kusumoto K. Efficacy of Cultured Epithelial Autograft after Curettage for Giant Melanocytic Nevus of the Head. Plast Reconstr Surg Glob Open. 2018 Jun 19;6(6):e1827.より引用
現在開発中の新しい母斑治療法
母斑組織を切除せずに、不活化処理(細胞をすべて死滅処理)し、真皮再生に再利用する新しい治療法の開発を行っています。自家培養表皮は真皮がない部分には生着しない、という問題点を克服するために国立循環器病研究センター研究所、大阪工業大学、関西医科大学と共同で開発しました。この治療法は、健常な皮膚を採取することなく、切除した母斑組織そのものを用いて母斑がもともとあった部分の皮膚再生を行うことを目的としています。平成28年2月からこの方法を用いた初めての臨床研究「高圧処理により不活化した母斑組織の再移植と自家培養表皮を用いた色素性母斑に対する新規皮膚再生治療法」を関西医科大学で開始し、10例の患者さんを対象に治療の安全性と有効性を確認する臨床研究を実施しました。更に、この高圧処理を行う機器の医療機器としての承認、及び保険治療となることを目標とした医師主導治験を2021年7月に開始、2023年1月に終了しました。今後は高圧処理装置の医療機器承認を目指すと共に、骨や神経の再生にも応用する予定です。
皮膚の再生医療について(研究についてもご覧ください)
iPS細胞の登場もあり、再生医療は注目を集めています。皮膚の再生医療は最も古くから臨床応用された分野であり、他人の皮膚移植(同種皮膚移植)は1950年代から、自家培養表皮は1970年代に、二層性人工真皮は1990年代に開発されています。しかし、残念ながら完全な皮膚再生は未だに不可能です。私は皮膚再生研究を20年近く行っており、培養皮膚、薬剤徐放性新規人工真皮(2018年ペルナックGプラスとして保険収載)の開発を行ってきました。少しずつですが、皮膚再生の鍵は見つかってきています。治療は様々な技術を組み合わせることで進歩することが多く、皮膚再生も、自家培養表皮などの細胞、人工真皮、細胞成長因子(薬剤)、高圧処理(物理的工学処理)などの新規技術を組み合わせて今後も発展すると考えています。
色素性母斑の治療は、大きさや部位によって様々な方法が考えられますので、十分相談させていただいてから治療に入ります。また、セカンドオピニオンとして相談していただくのも選択肢を考える上で非常によいと思います。まずは外来を受診され、ご相談ください。
森本尚樹(水曜日外来担当)
・外来予約等については京都大学医学部附属病院代表(075-751-3111)までお問い合わせ下さい。
自家培養表皮を用いた母斑治療についての症例報告
- Maeda T, Morimoto N, Kakudo N, Kusumoto K. Efficacy of Cultured Epithelial Autograft after Curettage for Giant Melanocytic Nevus of the Head. Plast Reconstr Surg Glob Open. 2018 Jun 19;6(6):e1827.
- Morimoto N, Kakudo N, Kako A, Nishimura K, Mitsui T, Miyake R, Kuro A, Hihara M, Kusumoto K. A case report of the first application of culture epithelial autograft (JACE(®)) for giant congenital melanocytic nevus after its approval in Japan. J Artif Organs. 2018 Jun;21(2):261-264.
高圧処理を用いた新規母斑治療に関する論文一覧
- Morimoto N, Mitsui T, Sakamoto M, Mahara A, Yoshimura K, Arata J, Jinno C, Kakudo N, Kusumoto K, Yamaoka T. A novel treatment for giant congenital melanocytic nevi combining inactivated autologous nevus tissue by high hydrostatic pressure and a cultured epidermal autograft:First-in-human, open, prospective clinical trial. Plastic and Reconstructive Surgery in press.
- Mitsui T, Morimoto N, Mahara A, Notodihardjo SC, Le TM, Munisso MC, Kakudo N, Yamaoka T, Kusumoto K. High Hydrostatic Pressure Therapy Annihilates Squamous Cell Carcinoma in a Murine Model. Biomed Res Int. 2020 Mar 7;2020:3074742.
- Mitsui T, Morimoto N, Mahara A, Notodihardjo SC, Le TM, Munisso MC, Moriyama M, Moriyama H, Kakudo N, Yamaoka T, Kusumoto K. Exploration of the Pressurization Condition for Killing Human Skin Cells and Skin Tumor Cells by High Hydrostatic Pressure. Biomed Res Int. 2020 Jan 30;2020:9478789.
- Masuoka H, Morimoto N, Mahara A, Sakamoto M, Mitsui T, Kakudo N, Kusumoto K, Yamaoka T. Simple and efficient method for consecutive inactivation-cryopreservation of porcine skin grafts. J Artif Organs. 2020 Jun;23(2):147-155.
- Le TM, Morimoto N, Mitsui T, Notodihardjo SC, Munisso MC, Kakudo N, Kusumoto K. The sustained release of basic fibroblast growth factor accelerates angiogenesis and the engraftment of the inactivated dermis by high hydrostatic pressure. PLoS One. 2019 Feb 21;14(2):e0208658.
- Sakamoto M, Morimoto N, Jinno C, Mahara A, Ogino S, Suzuki S, Kusumoto K,Yamaoka T. Melanin pigments in the melanocytic nevus regress spontaneously after inactivation by high hydrostatic pressure. PLoS One. 2017 Nov 1;12(11):e0186958.
- Morimoto N, Mahara A, Jinno C, Ogawa M, Kakudo N, Suzuki S, Fujisato T,Kusumoto K, Yamaoka T. The superiority of the autografts inactivated by high hydrostatic pressure to decellularized allografts in a porcine model. J Biomed Mater Res B Appl Biomater. 2017 Nov;105(8):2653-2661.
- Morimoto N, Jinno C, Mahara A, Sakamoto M, Kakudo N, Inoie M, Fujisato T, Suzuki S, Kusumoto K, Yamaoka T. The Alteration of the Epidermal Basement Membrane Complex of Human Nevus Tissue and Keratinocyte Attachment after High Hydrostatic Pressurization. Biomed Res Int. 2016;2016:1320909.
- Morimoto N, Jinno C, Sakamoto M, Kakudo N, Yamaoka T, Kusumoto K. An Exploratory Clinical Trial of a Novel Treatment for Giant Congenital Melanocytic Nevi Combining Inactivated Autologous Nevus Tissue by High Hydrostatic Pressure and a Cultured Epidermal Autograft: Study Protocol. JMIR Res Protoc. 2016 Aug11;5(3):e162.
- Morimoto N, Jinno C, Mahara A, Kakudo N, Fujisato T, Kusumoto K, Suzuki S,Yamaoka T. Verification of the Inactivation of Melanocytic Nevus in vitro Using a Newly Developed Portable High Hydrostatic Pressure Device. Cells Tissues Organs.2016;201(3):170-9.
- Morimoto N, Mahara A, Jinno C, Ogawa M, Kakudo N, Suzuki S, Kusumoto K,Fujisato T, Yamaoka T. An evaluation of the engraftment and the blood flow of porcine skin autografts inactivated by high hydrostatic pressure. J Biomed Mater Res B Appl Biomater. 2017 Jul;105(5):1091-1101.
- Liem PH, Morimoto N, Mahara A, Jinno C, Shima K, Ogino S, Sakamoto M, Kakudo N, Inoie M, Kusumoto K, Fujisato T, Suzuki S, Yamaoka T. Preparation of Inactivated Human Skin Using High Hydrostatic Pressurization for Full-Thickness Skin Reconstruction. PLoS One. 2015 Jul 30;10(7):e0133979.
- Jinno C, Morimoto N, Mahara A, Liem PH, Sakamoto M, Ogino S, Kakudo N, Inoie M, Fujisato T, Kusumoto K, Suzuki S, Yamaoka T. Inactivation of Human Nevus Tissue Using High Hydrostatic Pressure for Autologous Skin Reconstruction: A Novel Treatment for Giant Congenital Melanocytic Nevi. Tissue Eng Part C Methods.2015 Nov;21(11):1178-87.
- Morimoto N, Mahara A, Shima K, Ogawa M, Jinno C, Kakudo N, Kusumoto K,Fujisato T, Suzuki S, Yamaoka T. The rapid inactivation of porcine skin by applying high hydrostatic pressure without damaging the extracellular matrix.Biomed Res Int. 2015;2015:587247.
- Mahara A, Morimoto N, Sakuma T, Fujisato T, Yamaoka T. Complete cell killing by applying high hydrostatic pressure for acellular vascular graft preparation.Biomed Res Int. 2014;2014:379607.
